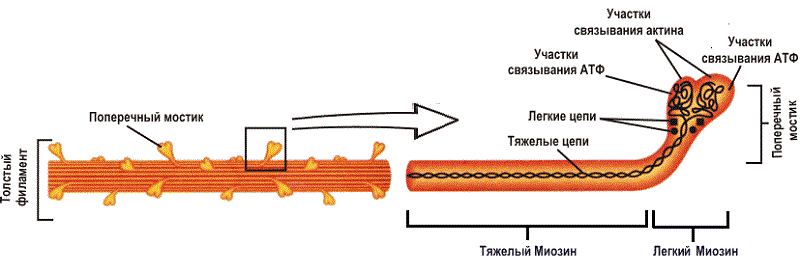
Основными миофибриллярными белками, составляющими до 55-60% от общего количества миофибриллярных белков, являются миозин (около 42%) и актин (около 16%). Кроме них, к миофибриллярным белкам относятся тропомиозин, тропонин и актинин. Однако по отношению к общей мышечной массе актин имиозин составляют лишь около 7-8%, и в мышцах содержится только около 70 г растворимого белка (актина и миозина) на килограмм. Актин и миозин также известны как миофиламенты и отвечают за сокращение и расслабление мышц.
Саркоплазматические белки насчитывают около 90 различных видов, основными из которых являются альбумины и глобулины. Альбумины полностью растворимы в воде, тогда как глобулины растворимы только в слабых растворах соли и нерастворимы в чистой воде. Миоглобин, придающий красный цвет мышечной ткани, и гемоглобин, обусловливающий цвет крови, являются наиболее важными представителями глобулинов. Саркоплазматические белки отвечают за метаболизм в клетках животных тканей. Основным представителем группы белков соединительной ткани является коллаген (40—60%) и некоторое количество тропоколлагена, присутствует также эластин (около 10%). Следовательно, значительная часть соединительной ткани, около 30%, состоит из других нерастворимых белков. Миофибриллярные белки денатурируют при 67-72 °С, тогда как температура денатурации саркоплазматических белков составляет примерно 62-70 °С, хотя некоторые саркоплазматические белки денатурируют уже при 50 "С. Соединительная ткань при 60—65 °С сжимается, уменьшаясь в размерах, а продолжительное воздействие высокой температуры (до 90—95 °С) при высокой влажности приводит к переходу коллагена в желатин. Как упоминалось ранее, после еще более длительной термообработки желатин расщепляется на отдельные цепочки проколлагена.
Прочность связывания воды с мышечной тканью различна. Так, вода, связанная с белком, составляет 4—6% от общего количества влаги мышечной ткани. Эта часть воды связана настолько сильно, что не замерзает даже при температуре около -45 °С. Степень связывания воды, находящейся между миофибриллами исоставляющей около 55—60% от общего количества влаги, зависит от рН мяса. Такая связанная с фибриллами вода известна как иммобилизованная (удерживаемая) вода, но связи в этом случае слабее, чем при взаимодействии с белком. Вода, присутствующая в саркоплазме, составляет около 20-25%; она является свободной. И наконец, внеклеточная вода составляет 8—14% общего количества и находится с наружной стороны клеточных мембран в капиллярах.
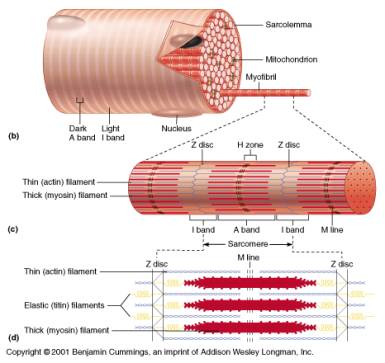
Сокращающиеся единицы мышечного волокна называются саркомерами. Бицепс человека насчитывает около 109 таких единиц. Саркомер, длина которого около 2 мм, располагается между двумя Z-линиями. Актин связан с Z-линией одним из своих концов. Миозин, с другой стороны, связан с М-линией. Зона частичного перекрывания миозина и актина получила название I-полоса, зона, в которой миозин и актин не накладываются друг на друга, — H-участок. Участок, соответствующий миозину, называют A-полосой. При описанном взаимном расположении актина и миозина на мышечном волокне под микроскопом видны поперечные полосы, а актин и миозин располагаются в виде гексагональной структуры.
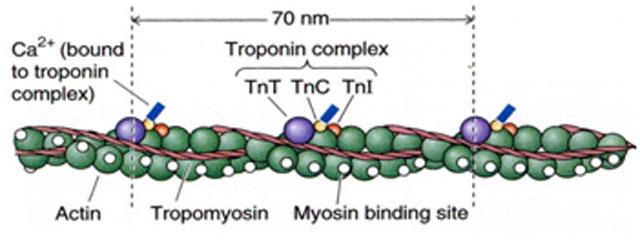
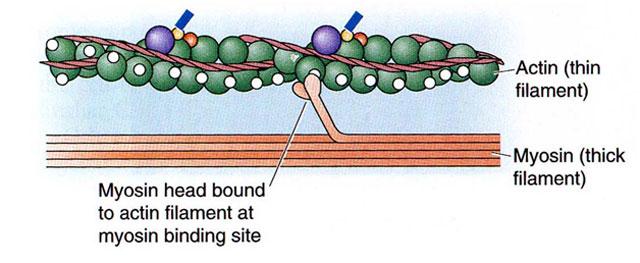
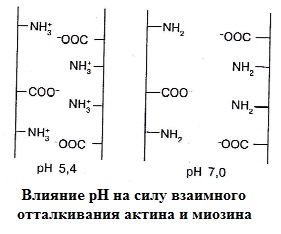
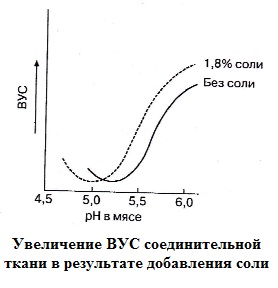
Снижение рН мяса до уровня рi приводит к снижению ВУС. В среде, близкой к pi актомиозинового комплекса, т. е. при рН 5,2, большинство групп —СООН находятся в виде анионов —СОО-, а большинство групп -NH2— в виде катионов —NH3+.
Положительно и отрицательно заряженные ионы притягиваются, и молекула белка прочно связана воедино. В таких условиях молекула белка имеет нулевой суммарный заряд, поскольку количество положительно иотрицательно заряженных групп в ней одинаково. В результате белок может связать лишь незначительное количество воды. Увеличение количества групп как с отрицательным, так и с положительным зарядом в белковой молекуле увеличивает ВУС мышечной ткани, поскольку в этом случае белок не так плотно упакован, как в изоэлектрической точке. Количество отрицательных зарядов превышает количество положительных при значении рН выше, чем pi белка, в этом случае ВУС увеличивается.
Волокна (филаменты) отталкиваются друг от друга, и пространство или зазор между актином и миозином увеличивается, что позволяет соединиться с белком большему количеству воды. В свежем мясе очень сходное явление можно наблюдать при значении рН ниже изоэлектрической точки, когда количество положительных зарядов превосходит количество отрицательных.
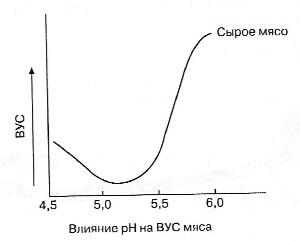
В тех случаях, когда аминогруппы присутствуют в мышечной ткани в виде нейтральных групп —NH2, связь между актином и миозином ослабевает. При ослаблении этой связи в волокнистой структуре может удерживаться большее количество воды; такая иммобилизованная вода не является свободной, она достаточно прочно связана. Таким образом, имеет место повышенное отталкивание между актином и миозином, в результате чего возникает капиллярный эффект, способствующий поглощению новых количеств воды. Капиллярный эффект можно сравнить с легким эффектом втягивания, который можно наблюдать, если поместить соломинку в стакан с водой: уровень воды в соломинке будет немного выше уровня воды в стакане. Положительное воздействие капиллярного эффекта на ВУС мышечной ткани заканчивается при значении рН около 6,4, поскольку отдельные волокна находятся настолько далеко друг от друга в этой точке, что эффект «втягивания» больше не проявляется. В целом повышенное значение рН (а следовательно, увеличение количества отрицательных зарядов) в мышечной ткани приводит к расширению зазора между актином и миозином вследствие усиления отталкивания и, в сочетании с капиллярным эффектом, приводит к тому, что мышечная ткань может связать больше воды.