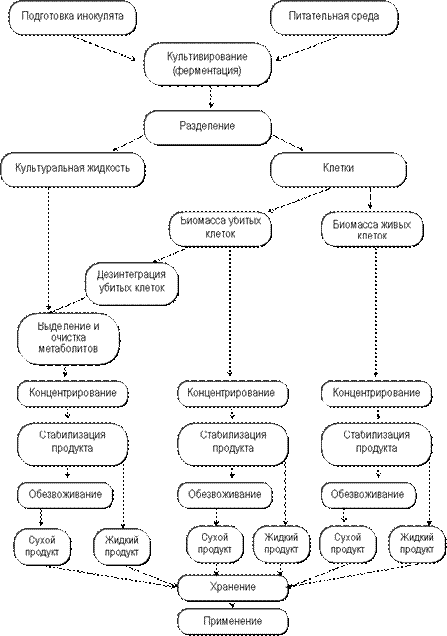
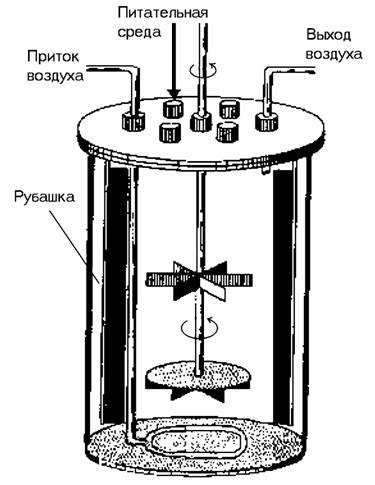
Виды хроматографии, двумерный электрофорез , ВЖХ, ультрацентрифугирование
Более тонкую очистку веществ осуществляют несколькими способами.
Наибольшее распространение получила хроматография. Каплю образца наносят на специальную бумагу (хроматография на бумаге) или пластинку стекла или пластмассы, покрытую тонким слоем инертного сорбента, например, целлюлозы или силикагеля (хроматография в тонком слое или тонкослойная хроматография). Затем такую пластинку одним концом помещают в смесь растворителей (например, воды и спирта).
По мере движения растворителей по пластинке, они подхватывают те молекулы образца, которые растворяются в них. Растворители выбирают таким образом, чтобы они связывались сорбентом по-разному. В результате молекулы образца, более растворимые в связанном растворителе, движутся медленнее, а другие, более растворимые в слабо сорбированном растворителе, движутся быстрее. Через несколько часов пластинку сушат, окрашивают и определяют положение различных молекул.
Можно разделять молекулы методом хроматографии на колонках (колоночная хроматография). В этом случае смесь молекул в растворе пропускают через колонку, содержащую твердый пористый матрикс. В результате взаимодействия с матриксом различные молекулы проходят через колонку с различной скоростью. После того как они достигнут в определенной последовательности дна колонки, их собирают отдельными фракциями.
В настоящее время разработано и применяется множество матриксов различных типов, используя которые можно делить белки согласно их:
заряду (ионообменная хроматография),
гидрофобности (гидрофобная хроматография),
размеру (хроматография гель-фильтрацией)
или способности связываться различными химическими группами (аффинная хроматография).
При ионообменной хроматографии нерастворимый матрикс содержит ионы, задерживающие молекулы с противоположным зарядом. Для разделения молекул используются следующие матриксы: диэтиламиноэтилцеллюлоза (ДЭАЭ-целлюлоза) - заряжена положительно; карбоксиметилцеллюлоза (КМ-целлюлоза) и фосфоцеллюлоза - заряжены отрицательно. Силы взаимодействия между молекулами в растворе и ионообменником определяются ионной силой и рН элюирующего раствора.
Гидрофобные колонки наполнены шариками, из которых выступают гидрофобные цепи; в таких колонках задерживаются белки с обнаженными гидрофобными участками.
Колонки, предназначенные для гель-фильтрации, заполнены крошечными пористыми инертными шариками; при использовании таких колонок происходит разделение белков по размерам. Молекулы небольшого размера по мере прохождения через колонку проникают внутрь шариков, а более крупные молекулы остаются в промежутках между шариками. В результате они быстрее проходят через колонку и выходят из нее первыми. В качестве матрикса можно использовать зерна поперечно-сшитого полисахарида (декстран или агароза).
Гель-фильтрация обычно используется и для разделения молекул, и для определения их размеров.
Гораздо более эффективен метод аффинной хроматографии (хроматография по сродству). В основе этого метода лежат биологически важные взаимодействия, происходящие на поверхности белковых молекул. При аффинной хроматографии используется нерастворимый матрикс, ковалентно связанный со специфичными лигандами (антителами или субстратом ферментов), которые присоединяют определенный белок.
Связываемые иммобилизованным субстратом молекулы фермента можно элюировать концентрированными растворами субстрата в свободной форме, а молекулы, связанные с иммобилизованными антителами, можно элюировать за счет диссоциации комплекса антитело-антиген концентрированными растворами соли или растворами низкого или высокого рН. Однократная хроматография на такой колонке позволяет зачастую достигнуть очень высокой степени очистки препарата.
Разрешение обычной колоночной хроматографии ограничено негомогенностью матриксов (например, целлюлозы), что вызывает неравномерное протекание растворителя через колонку. Разработанные недавно хроматографические смолы (в основу которых обычно положен кремний) имеют форму мельчайших сфер от 3 до 10 мкм в диаметре, которые упакованы в специальный чехол и образуют гомогенную колонку. Такие колонки для высокоэффективной жидкостной хроматографии (ВЖХ) обеспечивают высокий уровень разрешения. Поскольку частицы носителя в колонках для ВЖХ упакованы очень плотно, в отсутствие высокого давления скорость потока через них незначительна. По этой причине такие колонки обычно помещают в стальные цилиндры, соединенные со сложной системой насосов и шлангов, которые обеспечивают необходимое для высокой скорости протока давление.
В традиционной колоночной хроматографии скорость протекания через колонку может быть довольно низкой (примерно один объем колонки в час), таким образом, у разделяемых растворов достаточно времени для уравновешивания с внутренним содержимым крупных частиц матрикса. В условиях ВЖХ происходит быстрое уравновешивание растворов с внутренним содержимым крошечных сфер, так что растворы, обладающие различным сродством к матриксу, эффективно разделяются даже при высокой скорости потока. Таким образом, ранее для достижения плохого разделения с помощью колоночной хроматографии требовались часы, а в настоящее время благодаря ВЖХ качественное фракционирование занимает минуты. Вот почему именно этот метод чрезвычайно популярен сейчас для разделения и белков, и малых молекул.
Экстракты разрушенных клеток можно фракционировать, подвергая их высокоскоростному центрифугированию. Такая обработка делит клеточные компоненты по их размеру: более крупные частицы при центрифугировании движутся быстрее. Крупные компоненты экстракта, в том числе ядра или неразрушенные клетки, быстро оседают (седиментируют) при относительно низких скоростях и образуют осадок на дне центрифужной пробирки. Центрифугирование является, как правило, первым этапом фракционирования, с его помощью разделяются только значительно отличающиеся по размеру компоненты. Чтобы достигнуть более высокой степени разделения фракций, необходимо гомогенат наслоить тонким слоем поверх солевого раствора.
При ультрацентрифугировании различные фракции седиментируют с различной скоростью и образуют отдельные полосы, которые можно выделить. Во избежание перемешивания осажденных компонентов солевой раствор должен содержать инертный и хорошо растворимый материал (например, сахарозу), плотность которого постепенно увеличивается сверху вниз, формируя градиент плотности. При седиментации сквозь такие градиенты сахарозы различные компоненты клетки собираются в отдельные полосы, которые можно выделить.
Скорость седиментации каждого из компонентов определяется его размерами и формой и обычно выражается с помощью коэффициента седиментации, обозначаемого S. Скорость вращения до 80000 об/мин, так что на разделяемые частицы действуют силы, превосходящие силу тяготения более чем в 500000 раз. Под действием столь больших сил даже сравнительно небольшие макромолекулы, такие, как тРНК или простейшие ферменты, разделяются и распределяются в строгом соответствии со своими размерами. Измерение коэффициента седиментации макромолекулярных комплексов обычно используют для определения их общей массы и количества входящих в их состав субъединиц.
Ультрацентрифуга разделяет клеточные компоненты не только по массе, но и по плавучей плотности. В этом случае образец седиментирует в крутом градиенте, образованном высококонцентрированным раствором сахарозы или хлористого цезия. Компоненты клеток опускаются по градиенту до тех пор, пока не достигнут участка, плотность раствора в котором равна собственной плотности компонентов. Дальнейшей седиментации компонентов не происходит и они «застревают» на этом уровне. Таким образом в центрифужной пробирке возникает набор различных полос.
Метод центрифугирования в градиенте хлористого цезия был разработан в 1957 году для доказательства полуконсервативности репликации ДНК.
Электрофорез – метод разделения белков и нуклеиновых кислот в свободном водном растворе и пористом матриксе, в качестве которого можно использовать полисахариды, например, крахмал или агарозу. Биомолекулы обычно несут суммарный положительный или отрицательный заряд, обусловленный наличием на их поверхности положительно или отрицательно заряженных групп аминокислот.
Если белковые молекулы поместить в электрическое поле, они начинают перемещаться со скоростью, которая определяется их суммарным зарядом, а также формой и размерами. В середине 60-х годов был разработан модифицированный метод электрофореза - электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия (ДСН-ПААГ). При использовании данного метода белки мигрируют в инертном матриксе-полиакриламидном геле с высоким содержанием поперечных сшивок. Обычно гель готовят полимеризацией мономеров непосредственно перед использованием. Размеры пор геля могут быть подобраны произвольно с тем, чтобы гель мог замедлить миграцию определенных молекул. При этом белки находятся в растворе,содержащем мощный, отрицательно заряженный детергент - додецил-сульфат натрия или ДСН (SDS).Связываясь с гидрофобными участками белковой молекулы, этот детергент вызывает развертывание белковых молекул в длинные вытянутые цепи. Каждая молекула белка связывает значительное количество молекул детергента, приобретая суммарный отрицательный заряд. По этой причине белок после того, как будет приложено напряжение, начнет двигаться в направлении положительного электрода.
Белки одного размера ведут себя сходным образом, поскольку,во-первых, их природная структура полностью нарушена ДСН так, что их форма идентична, во-вторых, они связывают одинаковое количество ДСН и приобретают одинаковый негативный заряд. Крупные белки, обладающие большим зарядом, подвергаются действию значительных электрических сил, а также более существенному торможению. В обычных растворах эти эффекты, как правило, взаимно погашаются, но в порах полиакриламидного геля, действующего как молекулярное сито, большие молекулы тормозятся значительно сильнее, чем малые, поэтому оказываются ближе к стартовой линии. Смесь молекул делится на ряд полос, расположенных в соответствии с их молекулярной массой.
Выявить эти полосы можно путем окрашивания соответствующим красителем. Например, белки индентифицируются красителем кумасси синим. Известно, что близко расположенные полосы в геле могут перекрываться. Этот эффект препятствует выявлению большого количества белков (не больше 50) с помощью одномерных методов их разделения.
Метод двумерного гель-электрофореза, в котором объединены две различные процедуры разделения, позволяет идентифицировать более 1000 белков. Результаты при этом получают в виде «двумерной» белковой карты.
При работе данным методом на первом этапе белки разделяют по их заряду. Для этого образец помещают в небольшой объем раствора, содержащего неионный (незаряженный) детергент-меркаптоэтанол, и в качестве денатурирующего агента-мочевину. В этом растворе происходит солюбилизация, денатурация и диссоциация всех без исключения полипептидных цепей; при этом изменения заряда цепей не происходит.
Диссоциированные полипептидные цепи разделяют затем методом изоэлектрического фокусирования, основанном на изменении заряда белковой молекулы при изменении рН окружающей среды. Каждый из белков может быть охарактеризован изоэлектрической точкой - значением рН, при котором суммарный заряд белковой молекулы равен нулю, и, следовательно, белок не способен перемещаться под действием электрического поля. При изоэлектрическом фокусировании белки подвергаются электрофорезу в геле, в котором с помощью специальных буферов создается градиент рН. Под действием электрического поля каждый белок перемещается в ту зону градиента, которая соответствует его изоэлектрической точке и остается в ней.
Так происходит разделение белков в одном направлении двумерного гель-электрофореза. На втором этапе гель, содержащий разделенные белки, снова подвергается электрофорезу, на этот раз в направлении перпендикулярном тому, что на первом этапе. В этом случае электрофорез ведут в присутствии ДСН и белки разделяют по их молекулярной массе, как в одномерном ДСН-ПААГ. Исходный гель пропитывают додецил-сульфатом натрия и, поместив его на блок ДСН-ПААГ-геля, проводят электрофорез, в ходе которого каждая из полипептидных цепей мигрирует сквозь блок геля и образует в нем отдельную полосу. Неразделенными в результате остаются только те бели, которые неразличимы как по изоэлектрической точке, так и по молекулярной массе; такое сочетание встречается очень редко.
http://www.biotechnolog.ru/prombt/prombt5_6.htm